
Roche anuncia detalles de su estudio ‘fundamental’ para reducir la huntingtina
El ensayo GENERATION-HD1 probará si el RG6042, antes Ionis-HTTRx, ralentiza la progresión de la enfermedad de Huntington

Es un momento de grandes avances en el campo de los fármacos para reducir la huntingtina, cuyo objetivo es reducir la producción de la proteína huntingtina que causa la enfermedad de Huntington. En la reunión de la Red Europea de la Enfermedad de Huntington (EHDN) de la semana pasada, Roche anunció detalles concretos del primer estudio fundamental de un fármaco para reducir la huntingtina: el RG6042, que quizás conozca mejor como Ionis-HTTRx. ¿Qué sabemos del ensayo?
¿Qué es la reducción de la huntingtina?
En primer lugar, un breve resumen sobre la reducción de la huntingtina como tratamiento para la enfermedad de Huntington. Recuerde que el daño a los cerebros en la EH es causado por una proteína dañina, llamada huntingtina mutante. El gen de la EH, a veces llamado gen de la huntingtina, es una receta para fabricar la proteína huntingtina.

Cuando una célula necesita más de una proteína específica, por ejemplo, la proteína huntingtina, hace una especie de copia borrador del gen: una molécula mensajera que se escribe utilizando una sustancia química ligeramente diferente, llamada ARN. Debido a que este ARN lleva un mensaje, los científicos lo llaman ARN mensajero o ARNm. Cualquier rotura en esta cadena, desde el gen hasta el mensajero y la proteína, y la célula no fabricaría nada de esa proteína específica.
Así es como funcionan los enfoques de reducción de la huntingtina para tratar la EH: dirigiendo el ARN mensajero de la huntingtina y diciendo a las células que lo ignoren o lo eliminen. Menos mensaje, menos proteína.
La mayoría de los investigadores de la EH consideran que este enfoque es muy interesante, porque el sentido común y una gran cantidad de investigación con animales sugieren que si se reduce o elimina la proteína huntingtina mutante, se disminuye la gravedad de los síntomas de la EH.
ASO en la enfermedad de Huntington
Una de las primeras empresas en el campo de la reducción de la huntingtina es una empresa de biotecnología llamada Ionis Pharmaceuticals, de Carlsbad, California. Durante décadas, han desarrollado un enfoque llamado oligonucleótidos antisentido, que son moléculas muy modificadas similares al ADN que están programadas para reconocer solo un ARN mensajero específico que flota dentro de una célula.
Cuando estos ASO se adhieren a su objetivo programado, las células lo destruyen, reduciendo drásticamente los niveles de un ARN mensajero específico. Menos mensajero significa menos proteína, aunque el código genético del gen de la huntingtina siga estando ahí en el ADN.
Basándose en el éxito de las pruebas en animales, Ionis dirigió un estudio inicial en 46 valientes pacientes voluntarios con EH que comenzó en 2015. Este pequeño estudio fue diseñado solo para ver si su fármaco para reducir la huntingtina, llamado HTTRx, era seguro y si el tratamiento con HTTRx reducía la producción de la proteína huntingtina en el sistema nervioso. No podemos tomar una muestra de tejido cerebral, pero podemos medir los niveles de la proteína huntingtina mutante en el líquido cefalorraquídeo que baña el cerebro.
Como se comentó en HDBuzz, en diciembre de 2017, Ionis y su socio Roche anunciaron que el ensayo había sido un éxito. Sorprendentemente, ninguno de los 46 pacientes había abandonado el estudio, a pesar de las inyecciones mensuales en el líquido cefalorraquídeo necesarias. Y aún más notablemente, el tratamiento con HTTRx condujo a una sorprendente reducción en los niveles de la proteína huntingtina en el líquido cefalorraquídeo.
Roche es una gran empresa farmacéutica con sede en Suiza y su brazo estadounidense se llama Genentech. Junto con las buenas noticias del primer ensayo, Roche confirmó que planificaría y dirigiría el próximo ensayo de HTTRx, al que renombró RG6042 como parte del traspaso. Acostúmbrese a las historias sobre RG6042, pero recuerde que es el mismo fármaco HTTRx que hemos estado apoyando todo el tiempo.
Un ensayo para probar la eficacia
Por supuesto, tanto los investigadores como la comunidad de la enfermedad de Huntington están interesados en ralentizar la progresión de la EH, no en cambiar los niveles de alguna medición en el líquido cefalorraquídeo. Pero el exitoso estudio de seguridad de Ionis tuvo solo tres meses de dosificación en 46 pacientes, lo que es demasiado corto y demasiado pequeño para determinar si el tratamiento tuvo algún efecto en los síntomas de la EH.
“GENERATION-HD1 se lanzará a finales de 2018, con los primeros pacientes inscritos a principios de 2019. Se llevará a cabo en alrededor de 80-90 centros en unos 15 países.”
Ahora que sabemos que el fármaco de Ionis/Roche reduce la proteína y parece ser seguro, lo que necesitamos ahora es un estudio grande en un grupo mucho mayor de personas, llamado ensayo de fase 3, para determinar si el RG6042 ralentiza la progresión de la enfermedad de Huntington.
Desde diciembre, hemos estado esperando ansiosamente un anuncio sobre este ensayo más grande. ¡Y el 16 de septiembre lo recibimos!
GENERATION-HD1
En la reunión de la Red Europea de la Enfermedad de Huntington (EHDN) de 2018, Scott Schobel de Roche dio la primera visión general oficial del próximo estudio. El ensayo se conocerá como GENERATION-HD1.
(El nombre GENERATION-HD1 proviene de Global EvaluatioN of Efficacy and safety of Roche/genentech AnTIsense OligoNucleotide for Huntington’s Disease. Probablemente sea mejor recordar solo el acrónimo…)
El tamaño es importante
GENERATION-HD1 se lanzará a finales de 2018, con los primeros pacientes inscritos a principios de 2019. Se llevará a cabo en alrededor de 80-90 centros en alrededor de 15 países.
No se han hecho anuncios específicos sobre los centros, lo que significa que todavía no hay información pública sobre si alguna clínica o incluso país acogerá el estudio. Esperamos que esa información llegue pronto.
Será un estudio muy grande, que inscribirá a 660 pacientes con EH manifiesta. ‘EH manifiesta’ simplemente significa que se inscribirá a personas formalmente diagnosticadas con signos y síntomas clínicos de EH, no a personas con la mutación pero sin síntomas definidos (EH premanifesta o prodrómica).
Elegibilidad
Hay dos principales factores clínicos decisorios, o criterios de inclusión. En primer lugar, los pacientes deben ser «ambulatorios» y «verbales», es decir, capaces de caminar y hablar. En segundo lugar, deben obtener una puntuación del 70% o más en una prueba independiente llamada Evaluación Funcional. Eso significa un nivel de funcionamiento diario en el que puedan lavarse y realizar tareas domésticas «limitadas» como cocinar y usar un cuchillo.
Esos son criterios de inclusión clínica mucho más amplios que los del ensayo anterior, que estaba muy estrictamente limitado a la EH muy temprana con un funcionamiento diario casi normal.
También hay un requisito específico de que algo llamado puntuación CAP tiene que estar por encima de un cierto valor.
La puntuación CAP es una forma matemática sencilla de combinar la edad de una persona y su recuento de repeticiones CAG: la longitud del trozo anormal de ADN que causa la enfermedad de Huntington. Esta puntuación se utiliza porque las personas con mutaciones de EH más graves (repeticiones CAG más largas) tienden a tener síntomas de EH a una edad más temprana. Por lo tanto, si queremos seguir la progresión de los síntomas de la EH a lo largo del tiempo en una persona, tenemos que tener en cuenta tanto su edad como su tamaño CAG. Establecer un requisito de puntuación CAP mínima significa que el ensayo puede centrarse en las personas con más probabilidades de mostrar beneficios del fármaco, lo que lo hace lo más pequeño y rápido posible.
Muchas punciones lumbares
El ensayo incluirá un grupo de tratamiento con placebo o simulado, de aproximadamente un tercio de los participantes en el ensayo. Este grupo es absolutamente necesario para hacer frente al efecto placebo: el hecho de que participar en un ensayo como este hace que las personas se sientan mejor, e incluso funcionen mejor, incluso si el fármaco no funciona.
Los otros dos tercios de los participantes se dividirán en dos grupos, ambos recibiendo el fármaco activo. La mitad del grupo tratado recibirá el fármaco cada mes, y la otra mitad cada dos meses. Esto es emocionante, porque podría permitirnos tratar con menos frecuencia, si eso demuestra ser igualmente eficaz que la dosificación mensual.
Sin embargo, todos los participantes de cada grupo tendrán que someterse a inyecciones mensuales en el líquido cefalorraquídeo, cada mes, durante dos años. El grupo de placebo recibirá una inyección de placebo cada mes. El grupo de fármaco mensual recibirá el fármaco cada mes. Y el grupo de dos meses alternará entre inyecciones de fármaco y placebo. Eso significa que nadie sabrá a qué grupo ha sido asignado.
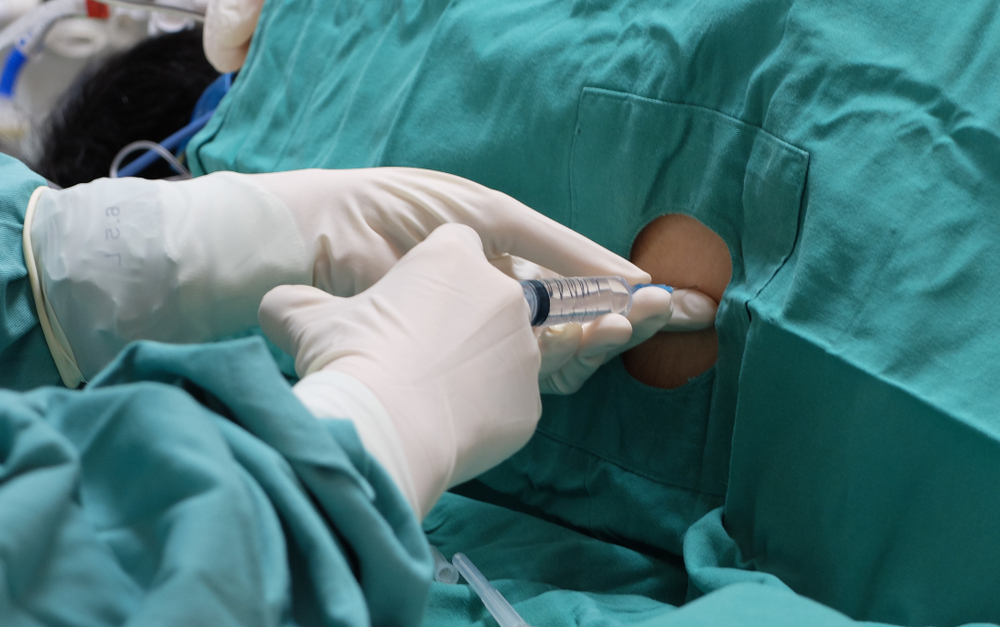
En resumen: todo el mundo en el ensayo tendrá que estar de acuerdo con recibir muchas punciones lumbares e inyecciones espinales, hasta veinticinco durante dos años.
Medidas de resultado
El éxito o el fracaso en el ensayo se determinará en los EE. UU. por algo llamado escala de capacidad funcional total, o TFC para abreviar. Esta es una escala de calificación muy simple basada en la capacidad de una persona para llevar a cabo tareas básicas en la casa, el trabajo y cuidarse a sí misma.
En Europa, el ensayo utilizará una medida ligeramente más sofisticada, llamada escala de calificación unificada compuesta de la enfermedad de Huntington o cUHDRS. Esta puntuación tiene en cuenta una gama más amplia de síntomas de la EH, combinando la TFC, una puntuación de movimiento y algunas pruebas de pensamiento.
“Será un estudio muy grande, que inscribirá a 660 pacientes con EH manifiesta.”
Es un poco inusual, pero no inaudito, tener un ensayo con diferentes criterios de valoración en diferentes países. Pero estas puntuaciones están midiendo el mismo proceso subyacente, que es el empeoramiento de la EH con el tiempo, y las diferentes agencias reguladoras parecen tener diferentes opiniones sobre la mejor manera de medir eso. Al final, esperaríamos que ambas puntuaciones se movieran en la misma dirección si el fármaco funciona.
No todos los pacientes se inscriben el primer día del ensayo, por lo que un ensayo en el que cada participante participa durante 25 meses tardará aproximadamente el doble en ejecutarse, y posiblemente más.
Pero espere, hay más
Roche también anunció otro estudio, llamado Estudio de Historia Natural, destinado a proporcionar información crucial sobre la progresión de la EH. Se inscribirán hasta 100 pacientes, emparejados con los participantes en el estudio de extensión de etiqueta abierta de RG6042 que ya está en curso. Esos participantes de etiqueta abierta son las personas del primer ensayo clínico, que ahora están recibiendo el fármaco regularmente, por lo que el estudio de historia natural ayudará a comprender los datos emergentes del estudio de etiqueta abierta. Si todo va según lo previsto, a los participantes en el estudio de Historia Natural también se les ofrecerá tratamiento de etiqueta abierta, después de 15 meses de participación, incluidas punciones lumbares regulares.
¡Y aún más!
La reunión de la EHDN incluyó actualizaciones sobre otros programas interesantes para reducir la huntingtina, incluidos Wave Life Sciences, PTC Therapeutics y Uniqure. En breve proporcionaremos actualizaciones sobre esos y otros detalles de la EHDN 2018.
¿Y ahora qué?
Tras el primer estudio que demostró la seguridad a corto plazo y la reducción exitosa de la huntingtina, ahora tenemos detalles sólidos sobre un estudio ‘fundamental’ para demostrar si el RG6042 funciona o no, y un cronograma muy claro sobre cuándo sucederá eso.
Es importante tener en cuenta que las personas que participen en GENERATION-HD1 tendrán un camino largo y desafiante por delante, y participar será un trabajo duro, física y mentalmente.
Inevitablemente, también habrá muchas personas que no puedan participar por una u otra razón. Si bien eso puede ser enormemente decepcionante para esas personas, el fármaco será probado por voluntarios de todo el mundo, y es importante tratar de recordar que el propósito del ensayo es probar el fármaco para todos y para las generaciones futuras, no para dar el fármaco a ninguna persona individual.
Dicho esto, esta es una gran noticia. Después de muchos años de trabajo de cientos de personas, finalmente tenemos un programa para comprender si el tratamiento con este fármaco para reducir la huntingtina, RG6042, podría beneficiar los síntomas de la EH.
Estamos muy entusiasmados con este anuncio y con el estado del campo de la reducción de la huntingtina en general. Creemos que es justo que los miembros de la comunidad de la EH se sientan de la misma manera. Manténgase atento a HDBuzz para obtener actualizaciones sobre este y otros desarrollos de ensayos.


