Conferencia sobre Terapias en la enfermedad de Huntington 2020 – Día 1
Informe de HDBuzz desde la Conferencia anual sobre Terapias en el Enfermedad de Huntington en Palm Springs


Nuestras nuevas escritoras Rachel Harding y Sarah Hernández informan desde la Conferencia sobre Terapias en la Enfermedad de Huntington, la mayor reunión anual de investigadores de EH.
Martes por la mañana – Genotipo y fenotipo de la EH
¡Buenos días desde el soleado Palm Springs! Estamos emocionados de estar aquí para la 15ª Conferencia Anual sobre Terapias de la EH. Este año, además de Ed y Jeff, nos acompañan las nuevas escritoras de HD Buzz: Dr. Rachel Harding y Dr. Sarah Hernández. Joel Stanton está trabajando en nuestra salida a Twitter en directo en nuestras publicaciones diarias.

La sesión 1 se llama «Genotipo y fenotipo», charlas centradas en cómo la mutación de la EH (genotipo) cambia los síntomas de la EH (fenotipo). El primero es el Dr. Seth Ament, que describe el trabajo de su laboratorio al tratar de mapear los primeros cambios que ocurren en las células cerebrales de los ratones con la mutación de la EH. Las células de nuestro cuerpo, incluido nuestro cerebro, tienen ADN que codifica más de 20,000 genes. Qué genes se activan o desactivan en una célula determinada marca cómo funciona esa célula. El laboratorio de Ament ha estado estudiando esta activación de los genes que se expresan, y se esfuerza por comprender los factores específicos que hacen que las células EH expresen diferentes conjuntos de genes, con la esperanza de que se pueda reparar.
Ament describe primero su trabajo mapeando los lugares donde la proteína huntingtina, el producto del gen de la EH, se adhiere al ADN. La forma más obvia de que la huntingtina podría cambiar los genes que se activan o desactivan es adherirse directamente al ADN. De hecho, la proteína huntingtina se adhiere a diferentes partes del genoma en ratones EH en comparación con los ratones normales. Esto sugiere que la huntingtina puede estar haciendo algo directamente al ADN que es importante para comprender la EH.
En los ratones con el gen mutado de la EH, la huntingtina se adhiere al ADN en lugares donde hay mucha acción: los genes se leen y se usan. Esto sugiere que la huntingtina mutada podría estar haciendo algo único en áreas donde los genes se usan activamente. ¿Podría este cambio en el hecho de que la huntingtina se adhiera al ADN en diferentes áreas ayudar a explicar cómo las células con huntingtina mutada consiguen que sus conjuntos de células estén ligeramente revueltos?
De hecho, las regiones a las que se adhiere la huntingtina en ratones con el gen mutado contienen los mismos genes que cambian en las células de EH, lo que sugiere que esto podría ser cierto. El equipo de Ament encontró una relación sorprendente: pueden predecir cuán activa o inactiva es una región determinada del ADN según cuán bien se adhiera a ella la proteína huntingtina.
A continuación, Ament describe los esfuerzos de su laboratorio por mapear qué genes cambian en los cerebros con EH. Las nuevas tecnologías asombrosas permiten a los investigadores mapear genes en células individuales. El laboratorio de Ament trabaja con estas técnicas en la Iniciativa BRAIN de los NIH. El laboratorio de Ament utilizó estas nuevas técnicas para examinar los cambios en más de 13,000 células individuales de cerebros de ratones con EH. Hay varios tipos diferentes de células en el cerebro, y el enfoque de Ament le permite mapear los cambios en cada uno de esos tipos de células por separado. Esto proporciona una imagen mucho más clara que simplemente mezclarlos y analizarlos juntos. Estos resultados muestran el camino hacia una comprensión mucho más refinada de lo que está sucediendo exactamente en cada tipo de célula, lo que podría ayudarnos a comprender cómo tratar cada tipo de célula individualmente.
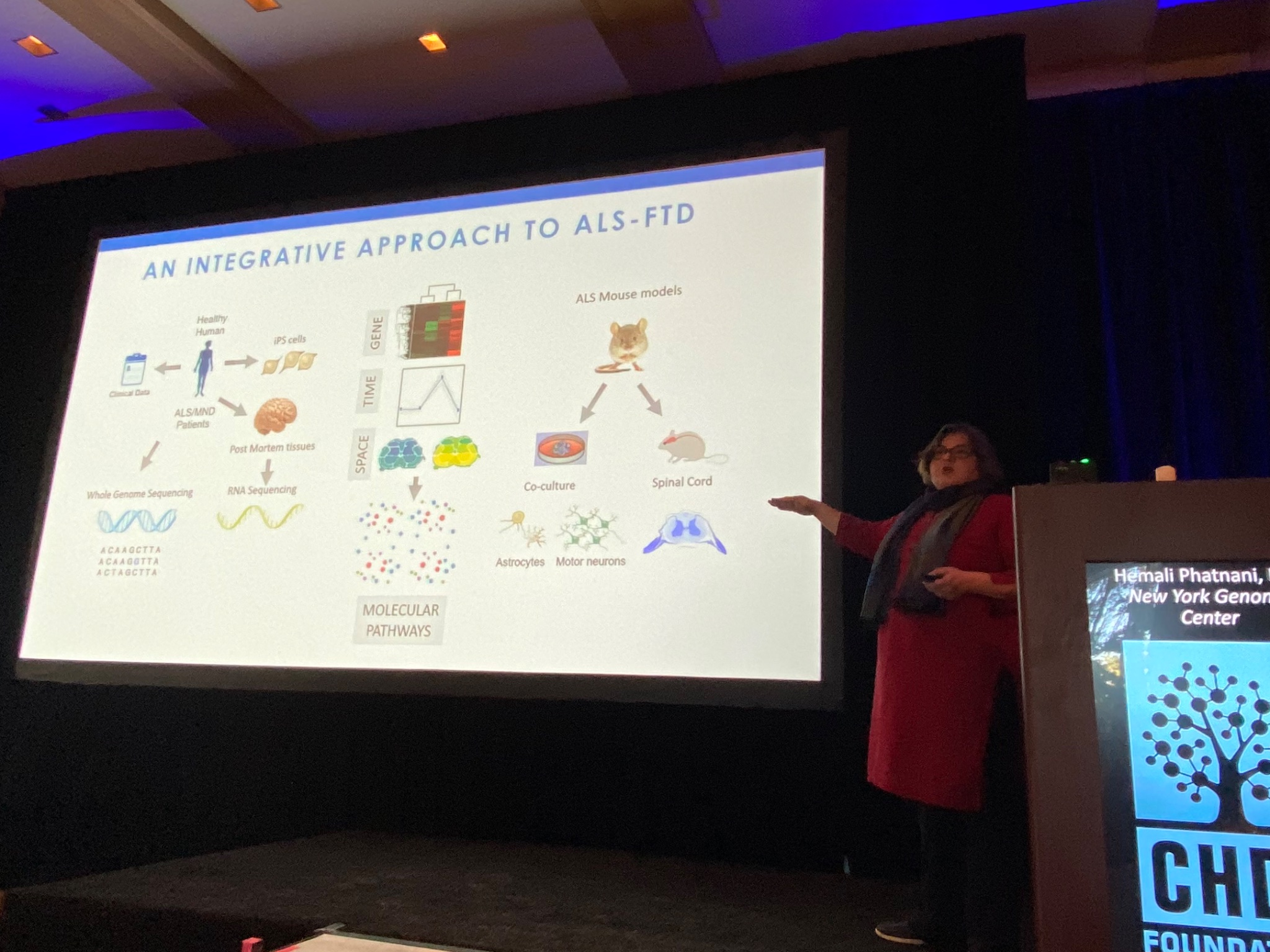
A continuación está Hemali Phatnani, del Centro de Genoma de Nueva York, quien describe su trabajo para comprender los cambios en el cerebro y la médula espinal de pacientes con ELA (enfermedad de Lou Gehrig) u otra enfermedad relacionada llamada FTD. Phatnani trabaja con un gran equipo de clínicas de ELA para obtener acceso a muestras raras donadas por pacientes con ELA. Estos se analizan y los datos se ponen a disposición de los investigadores de todo el mundo, ¡un gran modelo de ciencia abierta! Al igual que la EH, la ELA es una enfermedad compleja; diferentes tipos de células en el cerebro experimentan diferentes cambios durante el curso de la enfermedad. El equipo de Phatnani ha ayudado a desarrollar nuevos métodos para mapear los cambios en las células del cerebro de la ELA. Sus técnicas les permiten estudiar los cambios específicos de las células, y sus datos están disponibles para que cualquier investigador (o curioso no investigador) los explore en als-st.nygenome.org.
El siguiente es Sumanjit Jayadev del Centro Médico de la Universidad de Washington. Jayadev está interesado en estudiar un tipo particular de célula cerebral llamada microglia. La microglia juega un papel en la progresión de la EH, y deshacerse de la microglia en los modelos de ratón puede ayudar con los síntomas de la EH. Los científicos saben desde hace algún tiempo que la EH causa una respuesta inflamatoria, y Jayadev está interesado en qué células cerebrales (además de las neuronas) están jugando un papel en esta inflamación. Los genes involucrados en la inflamación son factores de riesgo para la enfermedad de Alzheimer (EA). Jayadev está buscando en qué células del cerebro están activados estos genes, para identificar el riesgo de enfermedad utilizando una técnica genial que proporciona datos a nivel de células individuales. Examinar estos cambios en las células individuales ha permitido a los investigadores identificar subtipos de microglia, y al observar estos subtipos se identificó un tipo particular de microglia solo presente en AD. Jayadev está trabajando en este proyecto con la gente de Sage Bionetworks que son expertos en ciencia abierta y datos abiertos en investigación biomédica. Con todos los datos generados, puede monitorizar la progresión de la enfermedad de AD al observar qué genes se activan dónde y cuándo. Esto puede ayudar a definir diferentes poblaciones de pacientes, lo que ayuda a los médicos e investigadores a comprender cómo funciona el proceso de la enfermedad. Si podemos aplicar esto a la EH, entonces quizás en el futuro al conocer la edad y la longitud del CAG de un paciente, los médicos podrían tomar decisiones informadas sobre cómo tratar a ese paciente específico.
La próxima charla es de William Yang, un investigador de la UCLA que estudia la EH. El Yang Lab genera muchos conjuntos de datos realmente grandes a partir de diferentes modelos de ratones EH, observando cómo se activan los diferentes genes, qué proteínas están presentes en diferentes tipos de células y reúne todos estos datos para comparar la EH con los controles. En estos grandes conjuntos de datos, los científicos pueden buscar patrones y correlaciones que podrían indicar cómo algunos genes trabajan juntos en modelos de ratones EH. Estos patrones se pueden mapear utilizando métodos computacionales para comprender cómo ciertos tipos de células en el cerebro contribuyen a los cambios en las expresiones genéticas que observan.
En esta charla, Yang se centra en el análisis que se realizó con ratones de control sin EH, donde su equipo demostró que esta técnica identificaba funciones importantes y qué tipos de células contribuyen a estas funciones. Cuando los datos del modelo de ratones EH se superponen en el mapa, encuentran que los genes que regulan los ciclos de sueño/vigilia y la reparación del ADN cambian, lo que confirma los hallazgos que los investigadores han hecho antes. Este mapa también se puede utilizar para probar muchas nuevas teorías que los investigadores tienen sobre la EH, ¡una herramienta bienvenida!
Martes por la tarde – Inestabilidad somática
La sesión de la tarde se centra en el proceso de inestabilidad somática. En pocas palabras, la inestabilidad somática ocurre cuando largas secuencias repetidas de ADN son inestables en ciertos tipos de células.
Primero esta tarde está Darren Monckton de la Universidad de Glasgow. Está interesado en estudiar cómo la inestabilidad somática puede conducir a Huntington y cómo atacar la inestabilidad podría ser una buena estrategia para crear nuevos medicamentos para la EH. Sabemos desde hace un tiempo que el número de CAGs puede variar en los tejidos y algunas células tienen longitudes mucho más largas que otras. Esto es similar a lo que vemos en otras enfermedades de expansión como la distrofia miotónica. La variación en el número de repeticiones de CAG aumenta a medida que los pacientes envejecen, lo que sugiere que hay más inestabilidad. Del mismo modo, cuanto mayor sea el número de repeticiones de CAG, mayor será la variabilidad y, por lo tanto, mayor será la inestabilidad. Vale la pena señalar que esto no significa que su número de CAG se alargue en general a medida que envejece, que seguirá siendo el mismo, solo significa que en algunas células, el número de repeticiones CAG a veces puede aumentar.
El CAG codifica el aminoácido glutamina, por lo que a veces escuchará llamar a la EH la enfermedad de poliglutaminas. Pero las glutaminas también pueden ser codificadas por CAA, por lo que aunque el ADN es diferente, la proteína que se produce será la misma con un CAG sustituido por un CAA. Esto sucede, por ejemplo, en el gen de la EH, donde una repetición larga de «C-A-G» crece más en los tipos de células más largas. Hay una publicación más detallada en HDBuzz sobre esto aquí.
Un reciente hallazgo interesante mostró que la presencia de CAA en algunos lugares en lugar de CAG es mejor para mantener la estabilidad del número de repeticiones. La siguiente pregunta interesante es: ¿qué está impulsando estos cambios que causan inestabilidad somática? La evidencia no apunta a la reparación del ADN, un tema candente en la reciente investigación de la EH.
La identificación de «drivers» (o genes) específicos de esta inestabilidad podría tener implicaciones terapéuticas para la EH. Los investigadores ahora están trabajando para averiguar cuáles de estos drivers son los más importantes en los pacientes, así como determinar cuáles son adecuados para desarrollar una nueva terapia o medicamento. Ahora los investigadores buscan ver cómo la inestabilidad o los cambios en la longitud del CAG varían en un paciente específico a lo largo del tiempo, todo gracias a aquellos pacientes que contribuyeron con muestras y datos en EnrollHD.
Si podemos monitorizar y rastrear la progresión de la EH midiendo la inestabilidad con un simple análisis de sangre, ésta podría ser una forma menos invasiva para que los médicos monitoricen la progresión de la enfermedad de los pacientes y sugieran la mejor manera de cómo podrían ser tratados.
El siguiente es Karen Usdin del NIH que ha estado observando la inestabilidad somática en modelos de ratón de una enfermedad diferente que afecta el sistema nervioso llamada X frágil. Al igual que la EH, la X frágil es una enfermedad de expansión de repeticiones, pero en lugar de expansión de CAG, en esta enfermedad se tiene una expansión de CGG. Podemos aprender mucho de otras enfermedades de expansión, ya que los científicos creen que hay muchas similitudes en los drivers de las enfermedades. También como la EH, la repetición de CGG que causa X Frágil se ve afectada por la inestabilidad somática, y los genes involucrados en la reparación del ADN influyen en este proceso. ¡Uddin está descubriendo, al menos en ratones X Frágil, que la alteración de los niveles de genes de reparación del ADN previene la expansión de la repetición CGG e incluso elimina algunas de las repeticiones! ¡Es fantástico escuchar a los científicos en esta reunión de fuera del campo de la EH, que comparten muchas ideas y conocimientos interesantes que podrían ayudar a impulsar la investigación de la EH más rápido!
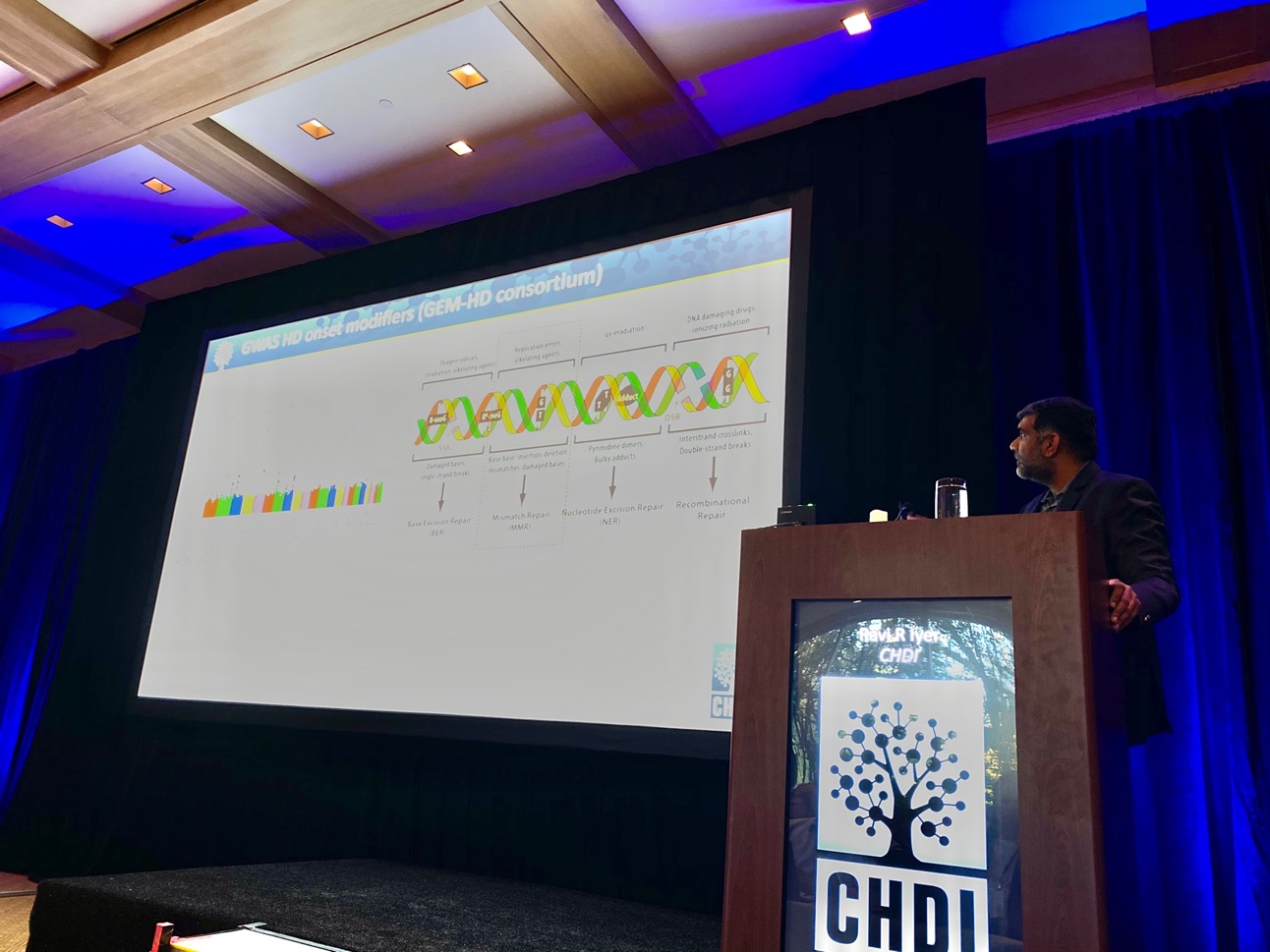
La última charla de la sesión es de Ravi Iyer, de CHDI, que analiza uno de los programas de descubrimiento de fármacos en los que los científicos están interesados. Uno de los objetivos de este programa de descubrimiento de fármacos es identificar moléculas pequeñas que estabilicen la expansión del CAG en la EH. CHDI está trabajando con muchas compañías diferentes para descubrir moléculas pequeñas usando muchas técnicas diferentes: la colaboración en estos difíciles proyectos ayuda a impulsar las cosas más rápido.
Una de las formas en que identifican las moléculas pequeñas que podrían funcionar es mirando modelos detallados de las estructuras de esas moléculas, como las proteínas involucradas en la reparación del ADN. La mejor parte de los programas que buscan identificar moléculas pequeñas es que podrían tomarse como una píldora si se demuestra que son tratamientos efectivos para la EH. Si bien la perspectiva del tratamiento con moléculas pequeñas es muy emocionante, los investigadores deben tener mucho cuidado de que las moléculas pequeñas que desean usar no tengan efectos secundarios inesperados.
Hacer moléculas pequeñas que podrían ser medicamentos para la EH es un proyecto emocionante, pero todavía estamos lejos de saber si esto tendrá éxito. Un gran equipo de científicos liderados por CHDI está trabajando duro para lograrlo y estamos entusiasmados de ver actualizaciones en las próximas reuniones.
Ahora estamos escuchando a Brian Bettencourt de Triplet Therapeutics, una de las muchas compañías que trabajan en este área, quien nos contará más sobre el objetivo terapéutico de la inestabilidad somática. Uno de sus objetivos es detener la inestabilidad somática de la expansión de CAG y retrasar el inicio de la EH, ¡con suerte a una edad tan avanzada que no es una vida realista! Esta ha sido un área de investigación tan prometedora que los científicos tienen que priorizar en qué moléculas trabajar primero. Esto les permite trabajar de manera eficiente hacia su objetivo de desarrollar terapias prometedoras para la EH lo más rápido posible. Después de priorizar candidatos por seguridad y bajo riesgo, el grupo de Bettencourt desarrolló moléculas que se dirigen a 8 genes diferentes. Si bien este es un gran número de objetivos, es un número lo suficientemente pequeño como para hacerse relativamente rápido. Nuevamente, esta investigación es parte de una colaboración más amplia, ya que Bettencourt está trabajando con Jeff Carroll de HDBuzz para estudiar estos diferentes objetivos terapéuticos potenciales. El grupo de Bettencourt debería informar sobre algunos de estos estudios el próximo año, así que estad atentos para ver si se puede utilizar la expansión somática para tratar la EH.
El último orador del día es el propio Jeff Carroll de HDBuzz, quien finalizará la sesión sobre inestabilidad somática. Una de las cosas en las que Carroll está interesado es comprender el efecto de reducir la huntingtina en el tejido no cerebral, como el hígado. Curiosamente, la reducción de huntingtina reduce la inestabilidad somática específicamente en algunos tejidos, pero no en otros. El laboratorio de Carroll quería entender estos hallazgos con más detalle, por lo que están colaborando con Sarah Tabrizi para buscar células neuronales humanas. La disminución de la Huntingtina en un modelo de ratón diferente que no tiene EH (pero tiene ataxia, una enfermedad de repetición de CAGs diferente) muestra que la inestabilidad somática también se reduce allí, lo que quizás sugiere que la proteína de la Huntingtina en general tiene un papel en la inestabilidad somática. Si la huntingtina está desempeñando un papel en la estabilidad del genoma y en el mantenimiento de nuestro ADN, el laboratorio de Carroll está dispuesto a determinar cómo podría estar sucediendo eso y cómo esto afectaría a los pacientes con EH. Esta es una observación muy nueva, ¡así que la gente está emocionada de explorar este hallazgo!
¡Y eso es todo para el día 1! Estén atentos a nuestros informes del día 2 y 3 y manténgase al día con la conversación en Twitter.