Desvelando el lado oscuro de la reparación de ADN para diseñar tratamientos para la EH
Un gen llamado MSH3 ayuda a reparar nuestro ADD, pero puede equivocarse y extender las repeticiones CAG en la EH. Los investigadores has desvelado nueva información sobre cómo se controla la actividad de MSH3, abriendo la puerta a nuevas terapias.
Un gen conocido como ‘MSH3’, que codifica una proteína implicada en arreglar y mantener nuestro ADN, se ha convertido en foco de interés en la investigación de la enfermedad de Huntington (EH), ya que actúa como una pieza clave en la enfermedad de múltiples estudios genéticos. En una reciente publicación, un equipo de científicos de la Universidad Nacional de Irlanda, en Galway, ha proporcionado pistas de cómo la proteína MSH3 está controlada en nuestras células, lo cual podría a ayudar a diseñar drogas destinadas a ralentizar of incluso prevenir la EH.
MSH3 – la espada de doble filo
La proteína MSH3 funciona corrigiendo los errores genéticos y protegiendo nuestros genomas contra las continuas agresiones al DNA que ocurren día a día. Lo hace escaneando nuestro ADN, buscando errores y reclutando otras proteínas para ayudar a arreglarlos en un proceso llamado ‘reparación de desajustes’.

Como puede saber, la EH es causada por una elongación inusual de repeticiones de las bases de ADN ‘C’- ‘A’- ‘G’ (los bloques de construcción del código genético) dentro de un gen llamado “huntingtina”. En las áreas del cerebro afectada por la EH, esta cadena de ADN repetido es ‘inestable’ – lo que significa que más unidades repetidas pueden ser agregadas a lo largo de la vida. Llamamos a este proceso ‘Expansión de ADN repetido’, o instabilidad somática. Para la mayoría de las enfermedades de expansión de repeticiones como la EH, cuanto mayor es la cadena, peores son los síntomas de la enfermedad.
Cuando MSH3 recorre esta repetición de CAG en nuestro ADN y reconoce un error, trata de arreglarlo, pero en su lugar inserta nuevas repeticiones, ¡lo que lo empeora!
¿Cómo podemos prevenirlo?
Si pudiéramos tener una droga que impidiera que MSH3 hiciera este error, podríamos desacelerar o prevenir el proceso de expansión de repeticiones, lo que debería reducir redujera la progresión de la enfermedad – o incluso detener la mortalidad…
¿Pero cómo podemos hacer esto sin interrumpir la función normal de MSH3 de proteger nuestro código genético? Normalmente, cuando los genes de reparación del ADN fallan, surgen toda clase de problemas por la acumulación de errores en el ADN – como el cáncer, por ejemplo.
Lo que es realmente interesante es que, a diferencia de otras proteínas de reparación del ADN conocidas por participar durante la expansión de repeticiones, la eliminación completa de MSH3 no parece tener muchos efectos secundarios adversos. Las células tienen un gran sistema de respaldo para cuando MSH3 no está – lo que hace de MSH3 una diana ideal para desarrollar medicamentos.
«Si pudiéramos hacer una droga que impidiera a MSH3 de cometer este error, podríamos desacelerar o prevenir la expansión de repeticiones, lo cual esperamos que reduzca la progresión de la enfermedad – o incluso parar la mortalidad»
¿Entonces que es nuevo?
Nuestras células pueden hacer que la proteína MSH3 funcione más lentamente al añadir una firma química llamada grupo acetilo, y hacerla funcionar más rápido al eliminar esta marca. Debido a que la expansión de repeticiones del ADN ocurre rápidamente cuando MSH3 está más activa, los científicos se proponen prevenir la eliminación del grupo acetilo. Estudios anteriores sugieren que una proteína llamada HDAC3 está implicada en la eliminación de este proceso. El grupo Laheu en la Universidad Nacional de Irlanda, en Galway, probó una droga en células humanas que frena la actividad de HDAC3, y observaron su efecto en la expansión de repeticiones de ADN.
¿Qué encontraron?
Encontraron que la droga previene la expansión de la repetición CAG en células humanas, y lo más importante, encontraron que no afecta a otras actividades importantes en la reparación del ADN, lo que sugiere que esta terapia no tendría consecuencias en el aumento del riesgo de cáncer.
Los investigadores también usaron esta droga para entender más sobre cómo HDAC3 controla la actividad de MSH3. Las proteínas tienen señales especiales llamadas “Secuencias de localización nuclear” (o ‘NLS’), las cuales actúan como un código postal que dirige la proteína al núcleo donde nuestro ADN se guarda. Encontraron que las marcas acetilo alteran el código postal de MSH3, dirigiéndola fuera del núcleo donde no puede mediar las expansiones de las repeticiones de ADN.
¿Qué significa todo esto?
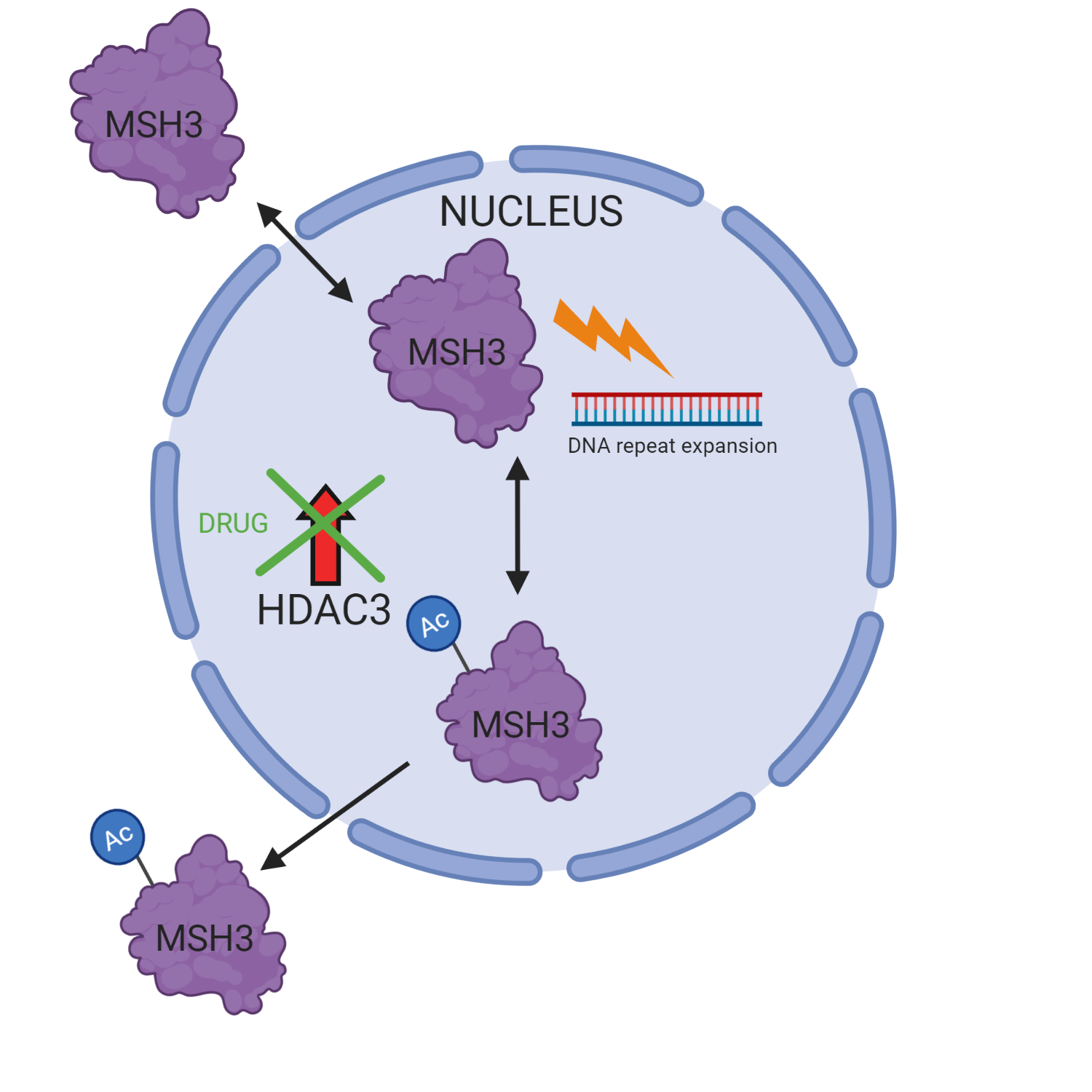
En general, el estudio sugiere un nuevo mecanismo regulador para la expansión de repeticiones del ADN a través de la eliminación de grupos acetilo de MSH3 por HDAC3. Esto puede proporcionar una explicación de por qué los pacientes con ciertas versiones de MSH3 tienen una progresión de la enfermedad más lenta, ya que por ejemplo sus grupos acetilo son más difíciles de eliminar.
Entender los mecanismos de la enfermedad de esta forma abre nuevas puertas para el diseño de drogas enfocadas a ralentizar la expansión del ADN (y de la enfermedad) – particularmente dado que los científicos de este estudio proponen que la inhibición de HDAC3 no afecta a la función principal de la reparación de desajustes en el ADN. La droga que usaron en este estudio es potente, selectiva y bien estudiada, así que parece ser una prometedora candidata para ensayos clínicos.
Dicho esto, intervenir las HDACs puede tener toda clase de efectos no deseados en las células. Necesitaríamos tener seguro que las drogas dirigidas a HDAC3 son inocuas con limitados efectos secundarios. Además, necesitaríamos ofrecer una forma de administrar el inhibidor de HDAC3 en las regiones más profundas del cerebro que están afectadas en la EH, lo cual es bastante difícil.
En resumen, este estudio es prometedor, pero es necesario mucho más trabajo antes de que podamos esperar esta droga como una terapia posible.