
Silenciando al mensajero con el silenciamiento génico de ARN monocatenario
Los nuevos fármacos de silenciamiento génico de ‘ARN monocatenario’ podrían ser más seguros y eficaces para tratar la enfermedad de Huntington
Tras enormes avances en los últimos años, nos acercamos cada vez más a los ensayos en humanos de la reducción de huntingtina o ‘silenciamiento génico’ como tratamiento potencial para la enfermedad de Huntington. Las técnicas más nuevas, mejores y seguras son siempre bienvenidas, y el anuncio del silenciamiento de ‘ARN monocatenario’ está causando bastante revuelo. ¿De qué se trata?
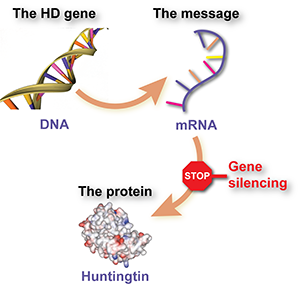
Los fármacos de silenciamiento génico actúan indicando a las células que no produzcan la proteína huntingtina, la causa del daño en la enfermedad de Huntington. Lo hacen interfiriendo con los sistemas de producción de proteínas de las células.
Existen dos tipos principales de fármacos de silenciamiento génico: oligonucleótidos antisentido (ASO) y interferencia de ARN (RNAi). Este artículo trata sobre la interferencia de ARN.
Mientras se avanza hacia los ensayos clínicos lo más rápidamente posible, los científicos también han estado trabajando en el desarrollo de una nueva y, con suerte, mejorada técnica de interferencia de ARN. Para explicar las diferencias con las técnicas existentes, necesitamos explicar un poco cómo se leen los genes para producir proteínas. Quédate con nosotros, ¡valdrá la pena!
¿Qué son el ADN y el ARN?
El ADN es el modelo para la fabricación de seres humanos. Es una molécula larga formada por trozos pegados llamados bases que vienen en 4 ‘sabores’: C A G y T. Estas son las letras en las que está escrito nuestro código genético.
La ‘doble hélice’ del ADN está formada por dos hebras que se alinean una al lado de la otra. Cada hebra es una cadena de bases, y las dos hebras se mantienen unidas por enlaces químicos entre las bases de las hebras opuestas. A se empareja con T, y C se empareja con G.
Para pasar del ADN a una proteína, es necesario hacer una ‘copia de trabajo’ del ADN. La copia se llama ARN ‘mensajero’, o ARNm. El ARN está estrechamente relacionado con el ADN, pero tiene un aspecto un poco diferente.
El ARNm es la plantilla que le dice a una célula cómo ensamblar una proteína. Siempre que una célula produce cualquier proteína, incluida la proteína huntingtina, lo hace leyendo las instrucciones del ARNm que corresponde a esa proteína.
Interferir con el ARNm de la huntingtina, o ‘silenciar al mensajero’, impide que se ensamble la proteína huntingtina, y es la base del silenciamiento génico en la interferencia de ARN.
Vale, volvamos al silenciamiento génico
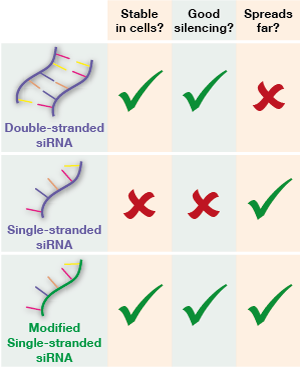
Hasta ahora, las técnicas de silenciamiento génico basadas en el ARN han utilizado moléculas de ARN de doble cadena, llamadas siARN. El ARN de doble cadena era necesario hasta ahora, porque el ARN de cadena sencilla es destruido por los propios mecanismos de eliminación de residuos de las células antes de que pueda realizar cualquier silenciamiento.
Una vez dentro de las células, el ARN de doble cadena necesita separarse en cadenas sencillas para permitir que se una a la molécula del mensaje del ARNm de la huntingtina. Entonces, una enzima de las células mastica el ARNm, de modo que la proteína mutante nunca llega a producirse.
Sabemos que esta forma de hacer las cosas puede disminuir drásticamente la cantidad de proteína HD mutante producida en las células. De lo que estamos menos seguros es de si la hebra no deseada que se separa tiene algún efecto secundario negativo en las células. Existe la posibilidad de que el cuerpo lance un ataque contra la hebra sobrante y cause daño. Otra posibilidad es que la hebra sobrante se una a otro ARNm e impida que se produzcan otras proteínas importantes.
Las moléculas de siRNA de doble cadena no se extienden mucho dentro del cerebro, lo que dificulta el tratamiento de grandes áreas cerebrales.
Una última dificultad de los siRNA de doble cadena es que deben empaquetarse de forma complicada para que lleguen a los tejidos adecuados para que hagan su trabajo.
Ha habido estudios en modelos animales de ratones y monos de la enfermedad de Huntington que demostraron que los siRNA son seguros y eficaces, pero los científicos somos un grupo cauteloso porque tenemos que estar realmente seguros de la seguridad antes de administrar cualquier tratamiento a los preciosos seres humanos. Lo último que queremos hacer es empeorar la EH.
siARN monocatenario
Una idea para reducir el riesgo de efectos negativos de la interferencia de ARN es producir un siRNA monocatenario. Pero, ¿cómo podríamos superar el problema de la estabilidad, esa molesta costumbre de las células de trocear el fármaco de ARN monocatenario?
Después de mucho trabajo duro, un grupo de investigadores dirigidos por David Corey en Dallas, en colaboración con ISIS pharmaceuticals, acaba de anunciar que finalmente lo han conseguido. Para que te hagas una idea de la emoción que esto ha causado, se anunció no en uno, sino en dos artículos ‘consecutivos’ en la misma edición de la revista de primer nivel Cell. ¡Todo un bombazo!
Mediante algunas modificaciones químicas de intentos anteriores, el equipo de Corey ha fabricado un siRNA monocatenario y ha podido empaquetarlo en una sencilla solución de agua salada. Inyectaron con éxito el siRNA monocatenario en los espacios fluidos que rodean el cerebro en un modelo de ratón de la EH, y pudieron demostrar que se une al ARNm de la huntingtina e impide que se produzca la proteína de la EH.
¿Ganar-ganar-ganar?
Además, a diferencia de los fármacos de siRNA bicatenario que se han probado antes, los efectos del siRNA monocatenario se extienden por todo el cerebro en lugar de limitarse a la pequeña zona cercana a la inyección. En estos ratones al menos, el siRNA monocatenario produjo un ganar-ganar: era estable y se extendía más.
No contentos con eso, fueron más allá. Al alterar ligeramente la estructura de su molécula, también pudieron crear un siRNA monocatenario que solo bloqueaba la producción de la proteína HD
Con un siRNA monocatenario no tenemos que preocuparnos por lo que pueda estar haciendo una segunda hebra, y al dirigirnos solo al ARNm de la huntingtina mutante, hay menos preocupación por los posibles efectos de detener la producción de la proteína HD normal.
¿Qué sigue?
Así que este nuevo método parece seguro y eficaz en modelos de ratón. Ahora tenemos que asegurarnos de que es seguro y eficaz en otros modelos animales más grandes antes incluso de considerar la posibilidad de pasar a los ensayos en humanos. ¡Eso está sucediendo ahora!
Preguntas pendientes
Habrá que responder a algunas preguntas antes de que la interferencia de ARN monocatenario pueda probarse en personas.
En primer lugar, hay otros genes con un tramo de CAG en ellos. Todavía no sabemos si la introducción de siRNAs monocatenarios dirigidos a esos tramos de CAG podría desactivar inadvertidamente otros genes importantes.
En segundo lugar, el problema de la administración. ¿Cómo vamos a llegar a las partes importantes del cerebro de los pacientes con la enfermedad de Huntington? Afortunadamente, los investigadores de la EH y otras enfermedades ya están trabajando en ello. Actualmente se está probando un fármaco similar fabricado con ADN monocatenario en la enfermedad de la neurona motora (ELA).
Por último, ¿cómo vamos a medir y controlar la eficacia del tratamiento? En los modelos animales, podemos hacerlo observando el tejido cerebral y midiendo la cantidad de proteína huntingtina que se produce. Esto es mucho más difícil de hacer en humanos, pero los mejores científicos están trabajando en ello y creemos que estamos listos para comenzar los ensayos en pacientes con la enfermedad de Huntington.
Más usos potenciales para el siRNA monocatenario
Un último adelanto de otro posible uso del siRNA monocatenario. Los investigadores también están estudiando su uso en combinación con la investigación con células madre. Básicamente, están trabajando en la toma de células de la piel de individuos con la enfermedad de Huntington, y en la conversión de esas células de la piel en neuronas. Esas neuronas podrían entonces ser tratadas con siRNAs monocatenarios para reducir los niveles de proteína HD dañina antes de trasplantarlas de nuevo al cerebro.
Pasarán muchos años antes de que la combinación de siRNA monocatenario con células madre derivadas de pacientes pueda utilizarse como tratamiento, pero es una idea ingeniosa y es bueno saber que se están explorando todas las vías. Mientras tanto, esperamos que el siRNA monocatenario avance con bastante rapidez hacia los ensayos clínicos.
Saber más
- Artículo de Cell de Lima y sus colegas que describe la técnica de siRNA monocatenario (el artículo completo requiere pago o suscripción)
- Artículo de Cell de Yu y sus colegas sobre el uso de siRNA monocatenario en ratones con la enfermedad de Huntington (el artículo completo requiere pago o suscripción)


