El silenciamiento del gen con ASO llega más lejos y dura más tiempo
Silenciar el gen de la EH utilizando ASOs alcanza más extensión, dura más y es seguro ¿Para cuándo estudios con human
Por Dr Nayana Lahiri 11 de noviembre de 2012 Traducido por Asunción Martínez Editado por Professor Ed Wild Publicado originalmente el 21 de junio de 2012
Los fármacos llamados oligonucleótidos anti-sentido, o ASOs, son una forma de silenciar el gen que produce la enfermedad de Huntington. Una nueva publicación en la revista Neuron sugiere que el silenciamiento del gen con ASOs alcanza más extensión del cerebro que otros métodos, dura más tiempo y es seguro.
Hemos estado esperando con gran ansiedad las novedades en el campo del silenciamiento del gen, por lo que estamos muy entusiasmados de leer hoy una nueva e importante investigación publicada en la revista Neuron. Un grupo de investigadores, dirigido por el Dr. Don Cleveland de la Universidad San Diego de California, junto con las compañías farmacéuticas Isis, Genzyme y Novartis, han estado desarrollando oligonucleótidos anti-sentido (ASOs) para la enfermedad de Huntington. Y, ¿qué que lo que han estado haciendo y qué es lo han encontrado?
Resumen genético

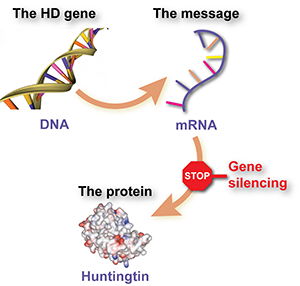
El gen de la enfermedad de Huntington es sólo uno de los aproximadamente 25.000 pares de genes, hechos de ADN, que llevan el código para fabricar proteínas, los bloques con los que las células construyen nuestros cuerpos. Hay un par de pasos entre el “código” de ADN y la proteína. Uno de estos pasos requiere al ARN mensajero o ARNm.
El gen de la EH es el código, que se traduce en ARNm de la EH. El ARNm es el que le dice a una célula cómo hacer la proteína huntingtina. Las personas que tienen la enfermedad de Huntington tienen una copia normal y una copia expandida del gen, así que también producen dos tipos diferentes de ARNm.
Desde que el gen de la EH fue identificado hace casi 20 años, los científicos han estado tratando de entender lo que hace, cómo produce los síntomas de la enfermedad y cómo podemos apagarlo de manera eficaz.
Desactivar el gen
Hay una serie de formas posibles de apagar el gen de la EH. Tal vez el más conocido es la interferencia del ARN, también conocido como ARNi o sARNi.
Otro enfoque utiliza una molécula ligeramente diferente llamada oligonucleótidos anti-sentido, o ASOs.
Los ASOs son algo similar a un cruce entre el ADN y ARNm. Son químicamente similares al ADN, pero están hechos de una sola cadena al igual que el ARNm. Al igual que otros fármacos de silenciamiento del gen, están diseñados para adherirse al ARNm de la EH y decirle a la célula que lo destruyan, evitando así que se forme la proteína huntingtina anormal.
Detrás de todo este trabajo subyace la teoría de que si se impide que se forme la proteína huntingtina anormal, se evitarán sus efectos dañinos en las células, y por lo tanto se disminuirán o retrasarán los síntomas.
En los últimos meses, hemos escuchado las novedades de varios grupos de investigadores que trabajan en el desarrollo de fármacos de ARNi, pero la publicación de noticias sobre investigación con ASOs son muy recientes. Esto ha cambiado con esta nueva publicación, que nos pone al día de varios años de duro trabajo.
Ya han comenzado los ensayos clínicos que utilizan ASOs en otras enfermedades neurológicas, pero en el caso de la EH se ha frenado porque tenemos algunas preguntas sin respuesta.
El efecto de los ASOs
En este nuevo trabajo, un grupo de investigadores inteligentes estudiado los efectos de la utilización de ASOs en 3 modelos diferentes de ratones con EH y también en un modelo de mono (lo más parecido a los humanos en términos de modelos animales), para encontrar las respuestas a una serie de preguntas distintas.
«Los ASOs llegan a zonas del cerebro que otras técnicas de silenciamiento del gen han sido incapaces de llegar »
En los monos, el fármaco se inyecta en el líquido espinal - un procedimiento mucho menos invasivo que la inyección en el cerebro, y que sería preferible para los pacientes humanos.
- 1. ¿Qué sucede cuando se infunden un ASO y cuánto tiempo dura?*
Bueno, pues infundieron un ASO en los ventrículos cerebrales (espacios llenos de líquido en el cerebro) durante dos o tres semanas. Esto condujo a la disminución de los niveles de la proteína huntingtina anormal a lo largo de muchas zonas que se sabe que son importantes en el cerebro, incluyendo el cuerpo estriado, que es la zona más afectada en la enfermedad de Huntington. Los ASOs eran capaces de extenderse mucho más allá en el cerebro de lo que lo hacen los fármacos ARNi.
Es más, los niveles se mantuvieron bajos durante mucho tiempo - hasta tres meses después de suspender la infusión.
- 2. ¿Qué pasó con los síntomas?*
Los investigadores son capaces de medir los síntomas de modelos animales mediante pruebas que miden los movimientos y el comportamiento. Los animales tratados con ASOs mejoraron en comparación con sus homólogos no tratados. Aún mejor, la mejoría se mantuvo durante mucho tiempo - y no sólo mientras los niveles de proteína eran bajos. Seguían habiendo mejoría de los síntomas algunos meses después de que los niveles de la proteína huntingtina anormal hubiera vuelto a los niveles previos al tratamiento.
Esto apoya la idea de que el cerebro sólo necesita un poco de ayuda, para hacer frente a los efectos del gen de la EH. Un destacado investigador de la EH, Carl Johnson, acuñó el término ‘vacaciones de la huntingtina’ para sugerir que un breve descanso de la proteína dañina puede ser todo lo necesario para inclinar la balanza a favor de la recuperación.
- 3. ¿Cuál es el mejor momento para administrar el tratamiento?*
Este estudio sugiere que posiblemente lo mejor sea administrar el tratamiento temprano.
Los síntomas motores en un modelo de ratón mejoraron dentro del primer mes de tratamiento y siguieron mejorando hasta que los ratones con la EH parecían iguales a los ratones normales. Los síntomas conductuales volvieron a la normalidad en los 2 meses de tratamiento.
Cuando se administró el tratamiento a los ratones sintomáticos más viejos, sus síntomas motores y de comportamiento mejoraron, pero tardaron más tiempo en que la mejoría fueran perceptibles y no mejoraron tanto como los ratones más jóvenes y sanos.
- 4. ¿Qué sucede si se bloquea el ARNm ‘normal’ de la EH?*
Esta es una de las principales preguntas que nos impiden empezar los estudios humanos en la enfermedad de Huntington. Sabemos que la proteína huntingtina es esencial para el desarrollo fetal, dado que los embriones de ratones diseñados para que no produzcan huntingtina no llegan a nacer. ¿Es seguro parar la producción tanto de la proteína normal como de la anormal en adultos?
Gracias a este trabajo, y el trabajo de otros investigadores sobre silenciamiento del gen, nos estamos acercando a una respuesta. La supresión de la producción del ARNm normal de la EH durante 3 meses en monos sanos fue bien tolerado. En los modelos animales de EH, al apagar tanto el ARNm normal como el ARNm anormal no cambió la cantidad de mejoría y no hubo ningún efecto perjudicial.
Ahora queda por resolver si los seres humanos pueden ser más sensibles que cualquier otro animal a tener menos huntingtina. Sólo un estudio con pacientes nos dará la respuesta con seguridad.
Esto es una buena noticia
Ahora sabemos que los ASOs pueden tratar partes del cerebro que otras técnicas de silenciamiento del gen no han sido capaces de alcanzar. No sólo eso, sino que una sola infusión con ASOs fue suficiente para retrasar la progresión de los síntomas en los modelos animales de enfermedad de Huntington a corto plazo. Y la reversión de los síntomas dura mucho más tiempo de lo esperado, incluso después de que los niveles de la proteína huntingtina anormal volvieran a la normalidad.
¿Y ahora qué?
Sabemos que las personas que son portadoras del gen expandido de la EH pueden permanecer muchos años perfectamente sanos, a pesar de que se produce proteína huntingtina anormal desde el nacimiento.
Tal vez un único tratamiento con ASOs, o el tratamiento anual, será suficiente para “reajustar el reloj de la enfermedad” bloqueando la producción de la proteína huntingtina durante el tiempo suficiente para que las células sean capaces de eliminar su acumulación. El siguiente paso en la investigación de este grupo será observar el tiempo que dura una única inyección de ASO.
Este trabajo también sugiere que la infusión en el líquido cefalorraquídeo podría ser útil para la administración de los medicamentos ASOs. Esto sigue siendo incómodo, pero es mucho mejor que insertar tubos y bombas para administrar los fármacos directamente al cerebro.
También tenemos que calcular la cantidad de ASO que será necesaria para producir un efecto en los seres humanos, cuándo y durante cuánto tiempo se debe administrar y estar preparado para los efectos secundarios inesperados.
Parece que estamos cada vez más cerca de los ensayos humanos de silenciamiento del gen en la EH. Hay varios grupos diferentes todos a punto de realizar estudios y con ganas de ser los primeros en probar el fármaco en pacientes, por lo que es un momento realmente emocionante para el silenciamiento del gen en la EH.